Introduction
Ouvrir une porte, couper ses aliments, se brosser les dents… Toutes ces activités quotidiennes ont une chose en commun : elles nécessitent l’utilisation d’un outil.
L’Homme, avec ses capacités de préhension, est devenu un animal expert dans l’utilisation d’outils, au point que certains auteurs qualifient même celle-ci comme « un trait définitoire de l’espèce humaine » (Osiurak F., 2014). Plusieurs questions arrivent alors : l’Homme a-t-il des capacités d’utilisation d’outils uniques ? Le cas échéant, pourquoi les espèces non-humaines n’ont-elles pas développé les mêmes capacités ? Comment l’homme parvient-il à une utilisation d’outils aussi sophistiquée ? Quel est le substrat neuronal qui rend possible celle-ci ? L’équipe Cognition Outils Systèmes (COSy) du laboratoire Études des Mécanismes Cognitifs a fait de cette thématique l’un de ses axes de recherche principaux. Au travers de diverses méthodes, l’équipe s’intéresse à la question de ce qui permet (et même plébiscite chez l’Homme) l’utilisation d’un outil pour accomplir une tâche.
Utilisation d’outils et évolution de la cognition humaine
L’utilisation d’outils est considérée comme le sceau d’adaptations cognitives complexes, que l’Homme aurait réussi à accomplir à travers l’histoire de son espèce et qui lui donnerait un avantage adaptatif certain. Ainsi, comprendre les bases neurocognitives de l’utilisation d’outils nous permet de plonger dans les origines de la cognition humaine et son évolution, toujours en débat depuis la publication de La filiation de l’homme et la sélection liée au sexe par Darwin en 1871.
Tout d’abord, il est à noter que les espèces non-humaines utilisent elles aussi des outils. Les primates, certains oiseaux et même des insectes peuvent utiliser un outil pour explorer leur environnement, pour trouver de la nourriture, ou pour construire leur abri (Baber C., 2003). L’utilisation d’outils n’est donc pas l’apanage de l’Homme. Cependant, la fréquence et la spontanéité de l’utilisation humaine d’outils sont bien supérieures à celles de l’utilisation non-humaine d’outils. Le degré de sophistication de l’utilisation n’est aussi pas le même : alors que les hommes se servent d’un outil pour en créer un autre, qu’ils sont capables de résoudre des problèmes complexes liés à l’utilisation d’outils, qu’ils transfèrent les connaissances mécaniques acquises dans un contexte à un autre contexte, les animaux non-humains ont une utilisation d’outils beaucoup plus limitée en ne manifestant aucun de ces comportements (Penn D.C., Holyoak K.J., Povinelli D.J., 2008).
Sur un plan neuroanatomique également, humains et non-humains possèdent des systèmes cérébraux homologues rendant possible la préhension, localisés au niveau du lobe pariétal supérieur et du sillon intra-pariétal. Cependant, il existe là encore une spécificité humaine. En effet, une aire du lobe pariétal gauche (LIP-G), le gyrus supra-marginal (GSM), n’existe pas chez le singe et pourrait jouer un rôle central dans l’utilisation d’outils (Vingerhoets G., 2014). Cette aire pourrait être à la base même de la spécificité comportementale inhérente à l’utilisation humaine des outils.
Malgré un accord sur le fait que l’utilisation d’outils par l’Homme est différente de celle qui peut être observée dans le règne animal, dans une perspective évolutionniste, deux théories s’opposent pour envisager les spécificités humaines de l’utilisation d’outils.
La première théorie embrasse l’idée d’une continuité de nature entre les espèces et voit la différence entre les utilisations humaines et non-humaines d’outils comme une différence de degré et non pas de nature. Ainsi, les différences entre humains et non-humains seraient quantitatives et pas qualitatives : l’animal non-humain aurait des capacités cognitives similaires aux nôtres, simplement moins développées (Mcgrew W.C., 2005).
Pour la seconde théorie, au contraire, la différence est bien une différence de nature et pas de degré. Les partisans de cette théorie affirment qu’il est fallacieux de penser que deux comportements analogues sont forcément dus à des causes similaires et qu’il ne faut pas négliger les différences entre comportements animal et humain. Les humains posséderaient des capacités cognitives bien différentes de celles de l’animal, qui ne seraient pas une simple complexification de capacités communes (Povinelli D.J., 2000).
Modèles cognitifs de l’utilisation d’outils
La dichotomie que l’on trouve entre ces théories sur l’évolution des espèces trouve écho dans deux approches qui considèrent le fonctionnement cognitif permettant l’utilisation d’outils et qui adoptent des cadres épistémologiques opposés.
La première approche, appelée aussi l’approche basée sur la manipulation (Buxbaum L.J., Kalénine S., 2010), se fonde sur des modèles issus de la neuropsychologie et postule que l’utilisation d’outils est possible grâce à des connaissances sensorimotrices à propos de la manipulation des outils, stockées dans le lobe pariétal inférieur gauche. Cette connaissance est acquise grâce à des expériences précédentes et encode les paramètres du geste associé avec la manipulation d’un outil (posture de la main, position de la main dans l’espace, etc.). Cette approche se situe dans la droite ligne de la théorie de la continuité évolutionnaire et envisage la particularité neuroanatomique humaine comme une simple amélioration du système de préhension existant déjà chez le singe. Dans ce cadre, l’aire cérébrale LIP-G serait une évolution du système de préhension commun et permettrait de stocker des connaissances sur la façon dont les objets devraient être manipulés pour être utilisés comme outils. La particularité de l’utilisation humaine d’outils découlerait de l’évolution du système de préhension commun et serait une différence de degré et non pas de nature.
Par contraste, la seconde approche propose que nous utilisions, non pas des connaissances, mais plutôt du raisonnement pour utiliser des outils : c’est l’approche basée sur le raisonnement (Goldenberg G., 2013 et Osiurak F., 2014). Ce raisonnement sur les propriétés physiques des objets permettrait de générer des actions et se baserait sur des connaissances mécaniques abstraites stockées dans l’aire cérébrale LIP-G. Un autre système, le système de production, serait en charge de régler les relations entre la main et l’outil et serait supporté par le sillon intrapariétal (SIP). Selon cette approche, seuls les humains seraient capables de produire des raisonnements mécaniques complexes, ce qui expliquerait les spécificités énoncées précédemment, qui seraient issues d’une différence de nature et pas de degré avec les espèces non-humaines.
Comprendre alors le rôle exact de l’aire LIP-G et plus particulièrement de l’aire GSM, pourrait alors apporter des arguments en faveur de l’une ou l’autre de ces deux théories. Pour cela, les neurosciences cognitives ont un outil de choix à leur disposition : la neuro-imagerie ou imagerie cérébrale.
Neuro-imagerie et modèles cognitifs
L’utilisation de la neuro-imagerie et en particulier de l’Imagerie par Résonance Magnétique fonctionnelle, ou IRMf, nous offre une possibilité unique d’entrevoir les bases neuronales de la cognition humaine. Cette technique nous permet de localiser précisément les zones cérébrales qui sont particulièrement activées lors de la réalisation d’une tâche cognitive spécifique. Mais chercher à localiser uniquement pour établir une cartographie des fonctions cognitives dans le cerveau humain n’a finalement pas plus d’intérêt que l’étude des cartes phrénologiques établies par Franz Gall. La localisation permise par la technique d’IRMf doit nécessairement, pour permettre une compréhension de la cognition humaine, être reliée à des modèles théoriques du fonctionnement cognitif. C’est uniquement en interprétant les résultats de l’IRMf au regard d’une théorie que l’on peut en déduire des éléments intéressants les sciences cognitives. De plus, l’essor des techniques des vingt dernières années et la multiplication conséquente des études empruntant cette méthodologie créent le besoin de synthétiser les résultats obtenus sur un sujet donné, résultats qui peuvent parfois sembler manquer de consistance.
Nous illustrerons ici, à travers la question des bases neurocognitives de l’utilisation d’outils, ces points importants. Nous tenterons d’interpréter les résultats d’une méta-analyse portant sur un ensemble large d’études réalisées en neuro-imagerie, dans les cadres explicatifs fournis par les deux approches concurrentes présentées ci-dessus.
Méta-analyse et neuro-imagerie
Trente-cinq études portant sur l’utilisation d’outils et cherchant à en investiguer les bases cérébrales à travers une méthode de neuroimagerie (IRMf ou Tomographie par Émission de Positons) ont été sélectionnées. Ces études rassemblent 60 expériences différentes et 916 participants, qui réalisent des tâches ayant trait à l’utilisation d’outils, pendant que leur activité cérébrale est enregistrée. Le but du présent travail est d’analyser la consistance des résultats de ces expériences sélectionnées pour répondre à une question particulière et de révéler les résultats stables à travers une large proportion de ces expériences.
Pour cela, la méta-analyse conduite se base sur les résultats rapportés par chaque étude individuellement et utilise la méthode dite de l’estimation de la vraisemblance de l’activation. En reprenant les coordonnées stéréotaxiques des pics d’activation rapportées dans les études, il s’agit de calculer en chaque point d’un cerveau représenté dans un espace standard, une probabilité d’activation consistante à travers les expériences. Ensuite, lorsque des voxels1 voisins ont une forte probabilité d’activation consistante, la méthode permet alors de révéler des clusters, ou groupes de voxels, qui représentent une localisation convergente de l’activité cérébrale à travers les études sélectionnées (Eickhoff S.B., Bzdok D., Laird A.R., Kurth F., Fox P.T., 2012).
Questions et prédictions
Les études issues de la littérature se penchent sur plusieurs types de questions relatives aux bases neuronales de l’utilisation d’outils. Nous choisirons ici de ne présenter qu’une seule question, centrée sur la nature de la tâche, pour apporter des éléments quant aux origines neurocognitives de l’utilisation humaine d’outils d’une part et pour illustrer notre propos méthodologique d’autre part. L’intégralité de l’étude fait l’objet d’une publication en cours de révision (Reynaud E, Lesourd M., Navarro J., Osiurak F., en révision).
Un des critères permettant de grouper les questions des études sélectionnées est celui de la nature de la tâche que l’on demande au participant de réaliser.
Nous pouvons distinguer deux grands types de tâches :
ACTION : le participant doit comprendre l’action que l’outil réalise sur un objet
GESTE : le participant doit juger si une manipulation d’outil est correcte ou incorrecte
Sur ces deux types de tâches, les prédictions qui sont faites par les deux approches décrites plus haut sont bien différentes.
La première approche, basée sur la manipulation, postule que ce sont les mêmes connaissances qui sont récupérées en mémoire lorsque l’on doit comprendre une action réalisée avec un outil ou évaluer si le geste réalisé avec un outil est correct ou non. Dans les deux cas, on ferait appel aux connaissances stockées sur les manipulations à accomplir pour utiliser un outil. Les activités cérébrales correspondant aux tâches de nature ACTION et GESTE devraient donc être similaires et localisées, entre autres, dans l’aire LIP-G. Aucune différence ne devrait être observée lorsque l’on compare les activités liées à ces tâches.
Pour la seconde approche, en revanche, les processus qui sous-tendent ces deux tâches sont différents : les tâches ACTION font appel aux connaissances mécaniques, au raisonnement et devraient donc générer des activations de l’aire LIP-G. Les tâches GESTE font elles appel au système de production, localisé dans le SIP, mais ne devraient pas engager d’activation dans l’aire LIP-G, puisqu’elles ne font pas appel à des connaissances issues du raisonnement, mais simplement à des connaissances sur l’interaction égocentrée entre la main et l’outil.
Résultats
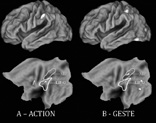
Après avoir établi des cartes cérébrales des zones activées de façon consistante pour les tâches ACTION et GESTE, nous avons ensuite réalisé une projection de ces cartes sur une surface corticale aplanie, afin de mieux visualiser les régions activées, souvent repliées sur elles-mêmes. La figure 1 représente les activations consistantes pour ACTION et GESTE.
Fig. 1 : Aires cérébrales activées par les tâches ACTION et GESTE, projetées sur une surface corticale 3D (en haut) ou aplanie (en bas). Les contours de LIP-G et de SIP sont tracés.
La figure 1 montre que l’aire LIP-G est significativement activée par les tâches ACTION, mais pas par les tâches GESTE.
Il existe également une activation de l’aire pariétale supérieure droite pour les tâches GESTE, mais pas pour les tâches ACTION.
Discussion
Nous souhaitions examiner, à la lumière des prédictions faites par les deux approches concurrentes de l’utilisation humaine d’outils, les résultats d’une méta-analyse en neuro-imagerie, afin de déterminer l’approche fournissant le cadre explicatif le plus satisfaisant.
Nos résultats montrent que l’activation cérébrale est différente pour les tâches ACTION et GESTE, ce que ne prévoit pas l’approche basée sur la manipulation.
Au contraire, nous mettons en évidence ici une activité supérieure pour les tâches ACTION par rapport aux tâches GESTE de l’aire LIP-G, comme le suppose l’approche basée sur le raisonnement : dans cette approche, seules les tâches ACTION demandent du raisonnement, alors que les tâches GESTE demandent de faire appel aux capacités permettant une posture manuelle appropriée. Ces capacités, selon cette approche, seraient localisées dans le SIP, région que nous retrouvons ici activée préférentiellement par les tâches GESTE par rapport à ACTION.
L’approche basée sur le raisonnement est donc la plus à même de rendre compte des résultats de notre étude et serait donc le cadre explicatif le plus plausible à l’utilisation humaine d’outils2.
Il semble donc que, pour utiliser des outils, nous raisonnons sur le monde physique qui nous entoure. Il a été montré que les singes sont incapables d’une telle faculté (Povinelli D.J., 2000). Ceci nous rendrait uniques dans notre utilisation d’outils et permettrait d’envisager l’évolution neurocognitive de l’homme en discontinuité par rapport à l’animal.
Ces résultats nous amènent également à repenser la considération parfois moindre que nous accordons au travail manuel. En effet, le terme de « travail manuel » laisse à penser que, pour se servir de ses mains et d’un outil, nous n’avons pas besoin de raisonner ou de faire appel à notre intelligence. Or, il semble qu’il ne puisse y avoir de « travail manuel » sans raisonnement : la hiérarchie implicite entre travaux manuels et intellectuels n’aurait donc pas lieu d’être.
Pour aller plus loin
Toutes les études incluses dans la méta-analyse concernent le sujet adulte, ni les bébés, ni les personnes âgées. Pour aller plus loin, et investiguer le raisonnement technique chez des populations différentes, nous renvoyons le lecteur vers d’autres études portant :
- sur le raisonnement chez l’enfant, ainsi que leurs possibilités en termes d’utilisation d’outils : Beck S.R., Apperly I. A., Chappell J., Guthrie C., & Cutting N. (2011). « Making tools isn’t child’s play », in Cognition, 119, 301- 306.
- sur la résolution de problèmes mécaniques dans la démence sémantique et la maladie d’Alzheimer : Lesourd M., Baumard J., Jarry C., Etcharry-Bouyx F., Belliard S., Moreaud O, Croisile B, Chauvrié V, Granjon M, Le Gall D, Osiurak F., (2015). « Mechanical Problem-Solving Strategies », in Alzheimer’s Disease and Semantic Dementia, Neuropsychology. 2015, Nov 2.
- sur la résolution de problèmes mécaniques chez les patients cérébrolésés à gauche : Jarry C, Osiurak F, Baumard J, Lesourd M, Etcharry-Bouyx F, Chauviré V, Le Gall, (2015). « Mechanical problem-solving and imitation of meaningless postures in left brain damaged patients: two sides of the same coin?», in Cortex. 2015, 63:214-6.
- sur la notion d’apraxie revisitée : Osiurak F., (2013). « Apraxia of tool use is not a matter of affordances », in Front Hum Neurosci, 2013 Dec 20;7:890.